Evaluación de las propiedades físicas del suelo y presencia de
micorrizas arbusculares en dos sistemas de cultivos de frijol (Phaseolus vulgaris y Phaseolus dumosus) en Sibundoy, Putumayo
Adriana del Socorro
Guerra Acosta3![]()
Recibido: 21/09/2025 Aceptado: 04/11/2025 Actualizado:06/04/2026
DOI: 10.17151/luaz.2025.62.10
Resumen
Los hongos micorrízicos arbusculares (HMA) pertenecen al filo Glomeromycota, estableciendo asociaciones mutualistas entre la mayoría de las plantas, generando beneficios como el aumento del crecimiento vegetal, la eficiencia en el uso de agua y nutrientes, y el control de patógenos. Este estudio evaluó la variabilidad porcentual de micorrización en dos sistemas agrícolas de Phaseolus vulgaris (fríjol voluble en suelo agrícola) y Phaseolus dumosus (fríjol tranca en suelo de conservación) en Sibundoy, Putumayo, a través de la caracterización de propiedades físicas del suelo, el conteo de esporas de HMA y el porcentaje de micorrización en raíces. Los suelos de conservación presentaron mayor densidad aparente (0,60 g·cm⁻³) y real (2,31 g·cm⁻³) que los suelos agrícolas (0,52 y 2,10 g·cm⁻³, respectivamente), así como mayor porosidad (75,16% frente a 73,51%). La humedad gravimétrica fue más alta en suelos de conservación (150,94%) que en los agrícolas (140,78%), al igual que la humedad volumétrica (77,31% vs. 64,85%). En cuanto a la conductividad hidráulica, se reportó moderada en suelos de conservación (4,18 cm·h⁻¹) y moderadamente lenta en los agrícolas (1,28 cm·h⁻¹). Se identificó un mayor número de esporas en suelos de conservación (52) comparado con los agrícolas (21), y un porcentaje de micorrización superior en P. dumosus (88,64%) frente a P. vulgaris (50,14%). Los resultados sugieren que las condiciones físicas del suelo y el tipo de manejo agrícola influyen significativamente en la presencia y efectividad de las HMA, lo que resalta su importancia ecológica y potencial aplicación en sistemas agrícolas sostenibles.
Palabras Clave: Densidad aparente, Densidad real, Humedad gravimétrica, Humedad volumétrica, Micorrizas, Propiedades físicas del suelo.
Assessment of soil physical properties and the presence of arbuscular
mycorrhizae in two bean cropping systems (Phaseolus vulgaris and Phaseolus
dumosus) in Sibundoy, Putumayo.
Abstract
Arbuscular mycorrhizal fungi (AMF) belong to the phylum Glomeromycota and form mutualistic associations with most plants, providing benefits such as increased plant growth, improved water and nutrient use efficiency, and pathogen control. This study evaluated the percentage variability of mycorrhization in two agricultural systems of Phaseolus vulgaris (common bean in agricultural soil) and Phaseolus dumosus (bush bean in conservation soil) in Sibundoy, Putumayo, through the characterization of soil physical properties, counting HMA spores, and determining the percentage of mycorrhization in roots. Conservation soils had higher bulk density (0.60 g·cm⁻³) and true density (2.31 g·cm⁻³) than agricultural soils (0.52 and 2.10 g·cm⁻³, respectively), as well as higher porosity (75.16% vs. 73.51%). Gravimetric moisture was higher in conservation soils (150.94%) than in agricultural soils (140.78%), as was volumetric moisture (77.31% vs. 64.85%). Regarding hydraulic conductivity, it was reported as moderate in conservation soils (4.18 cm·h⁻¹) and moderately slow in agricultural soils (1.28 cm·h⁻¹). A higher number of spores was identified in conservation soils (52) compared to agricultural soils (21), and a higher percentage of mycorrhization was observed in P. dumosus (88.64%) compared to P. vulgaris (50.14%). The results suggest that soil physical conditions and the type of agricultural management significantly influence the presence and effectiveness of AMF, highlighting their ecological importance and potential application in sustainable agricultural systems.
Keywords: Bulk density, True density, Gravimetric moisture content, Volumetric moisture content, Mycorrhizae, Soil physical properties.
Introducción
La micorrización es un proceso fundamental para la salud y productividad de las plantas, depende en gran medida de las propiedades físicas del suelo. Estas propiedades influyen en la capacidad del suelo para almacenar y conducir agua, interceptar y retener nutrientes, proporcionando un hábitat para microorganismos y facilitar la penetración de raíces (Carrillo et al., 2022). Las propiedades físicas del suelo, como la densidad, humedad y conductividad hidráulica, son claves para la colonización micorrícica, ya que afectan la disponibilidad de nutrientes y la retención de agua, factores esenciales para el desarrollo de los hongos micorrízicos y la salud de las plantas (Noda, 2009). Debido a su importancia, las micorrizas se consideran casi una relación obligada para el crecimiento vegetal en sistemas naturales y agrícolas (Osorio et al., 2019). Su uso se valora como herramienta de manejo sostenible del suelo, al favorecer la productividad de cultivos, la regeneración de comunidades vegetales degradadas y el equilibrio del ecosistema (Garzón, 2016).
Al respecto, Barrera (2009) afirma que, los hongos del suelo cumplen funciones clave en la nutrición y salud de las plantas, tanto en ambientes naturales como agrícolas. Entre ellos, destacan las micorrizas, asociaciones simbióticas entre hongos y raíces, cuyo nombre proviene del griego mikos (hongo) y rhiza (raíz) (Carrillo et al., 2022). Las micorrizas son asociaciones mutualistas entre hongos y raíces de plantas, donde ambos se benefician (Osorio, 2012). Facilitan la absorción de nutrientes, fortalecen la estructura de las comunidades vegetales y se integran funcionalmente a la planta sin causar daño (Lima et al., 2010). Además, contribuyen a la sostenibilidad del sistema suelo-planta y ayudan a mitigar la erosión (Lozano et al., 2015).
En la investigación se evaluó la presencia de micorrizas arbusculares en dos sistemas de cultivos de frijol, convencional con Phaseolus vulgaris (frijol voluble) y chagras tradicionales con Phaseolus dumosus (frijol tranca), así como las variaciones que se producen según la relación con la planta, el uso agrícola y algunas propiedades físicas del suelo (Gómez et al., 2024).
La investigación, tiene un enfoque cuantitativo y nivel descriptivo, con un diseño cuasi-experimental. Este diseño corresponde a una estrategia metodológica que busca analizar los efectos de determinados tratamientos o procesos de cambio en contextos donde los participantes o unidades de estudio se pueden seleccionan de manera aleatoria (Fernández et al., 2024) . El objetivo de la investigación fue evaluar las propiedades físicas del suelo –densidad aparente, real, porosidad, humedad gravimétrica, volumétrica y conductividad hidráulica– en dos sistemas de cultivo de frijol.
Materiales y métodos
La investigación se realizó en la vereda Tamabioy del municipio de Sibundoy Putumayo (Figura 1), con alturas entre los 2012 y 2055 m.s.n.m. corresponde a las coordenadas geográficas: 1° 10.884' de latitud norte y 76° 53.200'O longitud al oeste de Greenwich (Bello, 2016). Las condiciones climáticas de la zona de estudio son, temperatura promedio de 16 °C, humedad relativa cercana al 88 %, dentro de la zona de vida de Bosque Húmedo Montano Bajo (bh-MB) (Coorpoamazonia, 2007).
Figura 1. Mapa de
localización de las áreas de estudio ubicadas en las veredas, Villa Fátima,
Cabrera y Tamabioy del municipio de Sibundoy
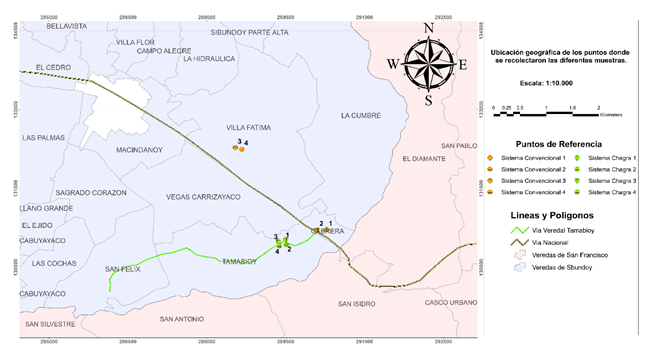
Fuente: elaboración propia.
Para el desarrollo de la investigación se usó un diseño cuasiexperimental comparativo, donde se tuvieron en cuenta dos tratamientos. T1: El frijol voluble que se encuentra en la chagra tradicional con Phaseolus dumosus (frijol tranca). T2: cultivo de Phaseolus vulgaris (frijol voluble) manejado de forma convencional, cada uno con cuatro lotes para un total de ocho (8) unidades experimentales.
Determinación de las propiedades
físicas del suelo
Las propiedades físicas evaluadas en campo se relacionan en la Tabla 1.
Tabla 1. Propiedades físicas
evaluadas en los dos sistemas de producción
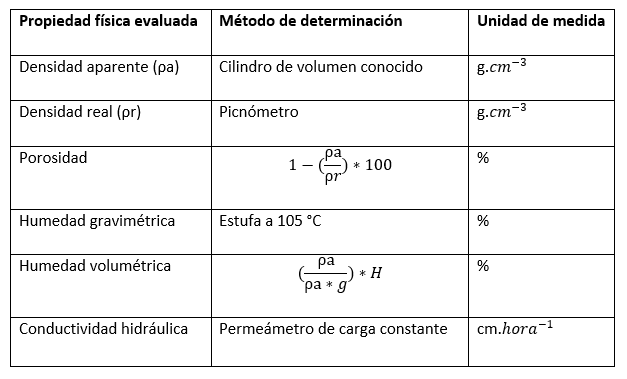
Fuente: elaboración propia.
Para evaluar los parámetros físicos de los suelos en cada unidad experimental (8), se elaboraron 4 cajuelas de 30 cm x 30 cm x 20 cm de profundidad, utilizando anillos de volumen conocido de 4,8 cm de diámetro, 2,5 cm de altura y 2 mm de grosor, además de suelos disturbados (Organización de las Naciones Unidas para la Alimentación y la Agricultura, 2024).
Por otro lado, para el aislamiento y conteo de esporas de hongos micorrízicos arbusculares (HMA), se utilizó el método propuesto por Gerdemann y Nicholson (1996, como se citó en Guerrero y Azcón, 2009), con las modificaciones allí descritas. El estudio se llevó a cabo en dos sistemas de manejo agrícola: cultivo convencional con Phaseolus vulgaris y chagras tradicionales con Phaseolus dumosus, cada uno con cuatro lotes experimentales. De cada lote se recolectaron 10 muestras de suelo, para un total de 80. Estas fueron secadas al ambiente durante 15 días, tamizadas (N° 10), y se tomaron 10 g por muestra. Cada muestra se mezcló con 1L de agua, se agitó, decantó y filtró con tamices de 425 µm y 63 µm. El precipitado se centrifugó con agua y luego con sacarosa al 50% (2700 rpm, 3 min), se lavó y se transfirió a cajas de Petri. Se observaron al estereomicroscopio (10X) únicamente esporas viables y turgentes, y se calculó el número por cada 10 g de suelo. El análisis fue realizado por triplicado.
Tinción y preparación de las
raíces para el estudio microscópico
Porcentaje de micorrización
Se recolectaron diez muestras de raíces de cada una de las unidades experimentales en ambos sistemas –convencional y chagra– para un total de 80 muestras de las especies evaluadas.
Etapa de laboratorio
Las raíces extraídas de diez plantas por unidad experimental se lavaron con agua potable hasta eliminar el suelo adherido, se dejaron secar a temperatura ambiente. Para la tinción se usaron los protocolos descritos por (Howeler y Sieverding, 2021)
La micorrización se estableció por la presencia de estructuras características de los HMA dentro de la raíz de la planta –arbúsculos, ensortijados, micelio interno o vesículas– según el protocolo de Howeler y Sieverding (2021)
Determinación y cuantificación del porcentaje de micorrización en
raíces
Para la evaluación del porcentaje de micorrización, se seleccionaron diez plantas por unidad de muestreo en cada sistema de manejo agrícola. A partir de cada planta se extrajeron 50 segmentos finos de la raíz principal para su procesamiento (Aguilar-Ulloa et al., 2016). Este procedimiento se aplicó de forma sistemática tanto en los lotes del sistema convencional de producción como en las chagras del sistema de conservación, abarcando un total de 40 unidades por sistema, para un total general de 80 muestras analizadas.
Las raíces fueron cuidadosamente lavadas para eliminar el suelo adherido, secadas a temperatura ambiente y segmentadas.
El procedimiento de tinción incluyó:
· Clarificación con hidróxido de potasio (KOH) al 10 % en baño serológico a 90 °C por 25 minutos.
· Decoloración con peróxido de hidrogeno (H₂O₂) al 10 % por 10 minutos.
· Acidificación con ácido clorhídrico (HCl) al 1 % durante 15 minutos.
· Tinción con azul de tripán al 0,05 % en baño a 90 °C por 10 minutos.
· Conservación temporal en glicerina al 50 % antes del montaje definitivo.
Montaje en portaobjetos
Los fragmentos de aproximadamente 2 cm fueron montados en portaobjetos (25 segmentos por lámina, dos láminas por muestra) y observados al microscopio óptico bajo aumento de 10x, siguiendo un conteo por transectos horizontales. Los fragmentos de raíz, de aproximadamente 2 cm de longitud, fueron montados en portaobjetos (25 segmentos por lámina, dos láminas por muestra) y observados al microscopio óptico con un aumento de 10X, siguiendo un conteo por transectos horizontales. El procedimiento se realizó a partir de raíces previamente aclaradas, teñidas y montadas conforme al protocolo establecido. Los segmentos fueron dispuestos de manera paralela y aleatoria sobre las láminas portaobjetos, a las cuales se adicionó el medio de montaje de polivinil-lactoglicerol (PVGL), empleado para el montaje de esporas o raíces procesadas previamente, y se cubrieron con cubreobjetos de 22 × 44 mm, según la metodología propuesta por Trouvelot (1986). Para cada muestra se prepararon 50 segmentos de raíz.
Durante la observación, se recorrieron las láminas realizando cinco transectos horizontales para evaluar la colonización en cada campo visual, desplazando la lámina en sentido horizontal con el carro portaobjetos del microscopio. El porcentaje de micorrización se determinó a partir de la observación de las estructuras características de las micorrizas —micelio interno, arbúsculos, vesículas o ensortijados—, considerando como campo colonizado aquel en el que se evidenciaron dichas estructuras, de acuerdo con los criterios descritos por Sierveding y Steven (1983). Finalmente, se contabilizó el número total de campos micorrizados observados.
El porcentaje de micorrización (%) se calculó con la fórmula:

Análisis estadístico
Para el análisis de las variables físicas del suelo y las micorrizas se realizó un análisis de varianza y pruebas de comparación LSD de Fischer, donde se encontraron diferencias significativas. Para ello se utilizó el software InfoStat Versión 2020e (Casanoves et al., 2022).
Resultados y discusión
El análisis de las propiedades físicas del suelo y la presencia de micorrizas arbusculares en los sistemas de cultivo evaluados permitió identificar diferencias significativas entre los tratamientos (P<0,05). A través de la caracterización edáfica, la cuantificación del número de esporas y la determinación del porcentaje de micorrización, se obtuvo información clave sobre las condiciones del suelo y su influencia en la simbiosis micorrícica (Pérez y Vertel, 2010). Los resultados obtenidos reflejan la variabilidad en la estructura y composición del suelo en función del manejo agrícola, evidenciando su impacto en la capacidad de colonización micorrízica. A continuación, se presentan los hallazgos derivados del análisis estadístico realizado.
Análisis de las propiedades
físicas
La prueba de significancia de LSD de Fischer de las propiedades físicas de los suelos evaluados en los sistemas de cultivo Phaseolus vulgaris y Phaseolus dumosus (Tabla 2).
Tabla 2. Comparación de medias para las propiedades físicas
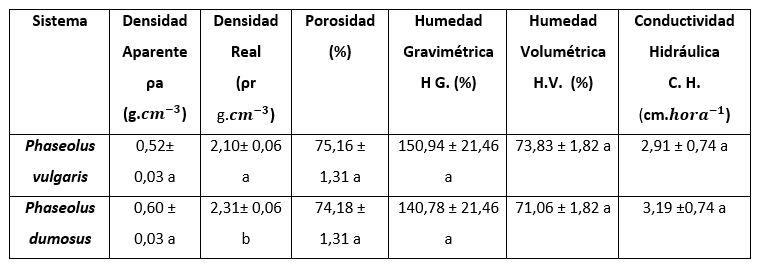
Fuente: elaboración propia
Densidad aparente (ρa)
Esta variable no presentó diferencias significativas (P<0,05), para los dos tratamientos evaluados.
El promedio de densidad aparente fue mayor en los suelos de chagras tradicionales (T2), con un valor de 0.60 g.cm⁻³, mientras que el sistema frijol convencional (T1), presentó un valor menor, de 0.52 g.cm⁻³. Esto ocurrió porque en el tratamiento T1 se empleó la caña de maíz como tutor, la cual, al ser incorporada al suelo al finalizar la cosecha, favoreció la acumulación de materia orgánica y en consecuencia, la reducción de la densidad aparente (Wang et al., 2025). En el estudio “Influence of soil organic matter decomposition on arbuscular mycorrhizal fungi” se reporta que la materia orgánica incrementa la longitud de raíces colonizadas AMF (Gryndler et al., 2009).
En general, se ha observado que un suelo con una densidad aparente menor y una estructura más abierta ofrece condiciones favorables para la colonización de hongos micorrízicos (González et al., 2015). Esta estructura más porosa facilita el movimiento del aire, el agua y los nutrientes, creando un entorno adecuado para el desarrollo de la biota del suelo. En particular, la presencia de poros más grandes y una menor compactación permite un mayor crecimiento y expansión de las hifas de los hongos, lo que favorece una interacción más estrecha con las raíces de las plantas (Drew et al., 2003). Esto puede resultar en un mayor porcentaje de micorrización, como resultado, se incrementa el porcentaje de micorrización, lo que mejora la eficiencia en la absorción de nutrientes esenciales y contribuye al fortalecimiento general de la salud y el crecimiento de las plantas (Hossne, 2008).
Según Salamanca y Sadeghian (2005), la ρa es una característica que influye en la productividad de los cultivos, ya que está estrechamente vinculada con otras propiedades del suelo. Esta característica impacta la estructura del sustrato influyendo en la ventilación, el drenaje y la retención de agua, elementos clave para el desarrollo de raíces y su relación con hongos micorrízicos (Callejas et al., 2009). Dado que se vuelve complejo una vez establecido, es esencial mantener una estructura física adecuada desde el inicio del cultivo (Nieto y Chegwin, 2010).
McGrath y Henry, (2016) afirman que la adición de materia orgánica reduce la densidad aparente porque introduce material de menor densidad y mejora la formación de agregados y la porosidad. Así como también Kefan et al. (2022) afirman que, la materia orgánica favorece la formación de agregados estables que aumentan la macroporosidad y reducen la compactación. Esto se traduce en menor densidad aparente.
Densidad real ρr.
El análisis de la densidad real del suelo presento diferencias estadísticamente significativas (P<0.05), los cultivos de frijol voluble (Phaseolus vulgaris ) con valor de 2,10 g.cm⁻³, los suelos de chagra con frijol tranca (Phaseolus dumosus), con valor de 2,31 g.cm⁻³.
Martínez y Roca (2011) mencionan que la densidad real es la relación entre la masa del suelo seco y su volumen sin incluir poros, y varía según la composición del sustrato. (Giap y Ahmad, 2024) señalan que la densidad real está determinada por factores físicos, químicos, biológicos, ambientales y de manejo del suelo. Es importante señalar que de acuerdo con Carrillo et al. (2022) una estructura suelta y porosa favorece la micorrización al mejorar la aireación y facilitar la colonización radicular; además, la baja densidad real se asocia a suelos con mayor porosidad y menor peso.
Del mismo modo, la densidad puede estar influenciada por varios factores. Por ejemplo, una estructura del suelo menos compactada y con mayor porosidad puede proporcionar un ambiente más favorable para el crecimiento de los hongos micorrízicos (Pire y Pereira, 2003). De esta manera, la presencia de una mejor aireación facilita la colonización de las raíces por parte de los hongos y promueve una interacción simbiótica más eficiente entre ambos organismos (Borie et al., 2000)
Porosidad
Los valores promedio fueron de 75,16 % para el cultivo de frijol convencional y de 74,18% para las chagras tradicionales, indicando que son suelos con excesiva porosidad >70 %. Por lo anterior la clasificación del espacio poroso, se debe a sus características de conducción o de almacenamiento de agua (Steponavičienė, et al., 2022). Al respecto Falcón et al. (2021) afirman que, la estructura menos compacta y con poros grandes favorece el crecimiento de hifas y su contacto con raíces, aumentando la micorrización y mejorando la absorción de nutrientes y la salud vegetal. De este modo, González et al. (2011) afirman que la porosidad del suelo, especialmente en los primeros centímetros, regula la infiltración, escurrimiento y el movimiento de agua y aire. Es un indicador de la calidad del suelo por su influencia en los intercambios físicos, químicos y biológicos (Correa et al., 2011).
Humedad gravimétrica
En cuanto a los estimativos se obtuvo el valor de 140,78 % para el suelo de la chagra tradicional y del 150,94 % para el suelo con cultivo de frijol voluble de manejo convencional. En este contexto, Cicore et al. (2015) afirman que, la humedad gravimétrica depende del equilibrio entre las fases del suelo e influye en la retención de agua, aireación y desarrollo vegetal. La materia orgánica mejora estas condiciones al favorecer la porosidad, los agregados y la retención hídrica (González et al., 2011).
Deepika y Kothamasi (2014) afirman que la humedad del suelo actúa como un filtro abiótico que regula la colonización por hongos micorrízicos arbusculares (AMF) y la diversidad de sus estructuras internas, ya que los suelos con exceso de agua presentan menor diversidad y colonización, mientras que las condiciones intermedias resultan más favorables. Asimismo, Shao et al. (2023) señalan que niveles de humedad moderados o estratégicamente controlados promueven el desarrollo del micelio extraradical y la colonización de las raíces, mientras que tanto el déficit hídrico extremo como la saturación excesiva reducen significativamente la actividad micorrízica.
Del mismo modo, Fernández et al. (2019) señalan que la capacidad de retención de humedad del suelo, influenciada por sus propiedades físicas, químicas y biológicas, resulta fundamental para el crecimiento y desarrollo de las plantas. En esta misma línea, Pauwels et al. (2023) evidencian que los hongos micorrízicos también pueden modificar las propiedades hidráulicas del suelo, mejorando su capacidad de retener agua. Esto refuerza la idea de que la interacción entre los componentes físicos y biológicos del suelo desempeña un papel determinante en la disponibilidad hídrica y, en consecuencia, en la productividad vegetal.
Humedad volumétrica
Esta variable no presentó diferencias significativas (P>0.05), los valores promedios obtenidos fueron para el cultivo de frijol voluble con 73,83 % y en la chagra con 71,06 %.
Una humedad volumétrica adecuada favorece la colonización micorrícica al crear condiciones propicias para el crecimiento fúngico, influenciada también por factores como temperatura, nutrientes y tipo de suelo (Pino et al., 2019). Además, la humedad volumétrica del suelo es un factor importante para la presencia y función de las micorrizas en las plantas (Mondragón y Haydee, 2015).
Conductividad hidráulica
Los resultados de esta propiedad fueron, para el cultivo de frijol convencional de 2,91 cm.hora⁻ ¹, mientras que para la chagra fue de 3,19 cm.hora⁻ ¹, no presentando diferencias significativas (P>0,05).
La conductividad hidráulica determina la velocidad del agua en el suelo; valores altos mejoran la infiltración y reducen erosión, mientras que valores bajos pueden generar anegamientos o erosión, según la topografía (Donald et al., 2011). Además, García et al. (2018) señalan que la conductividad hidráulica saturada influye directamente en procesos de infiltración, escurrimiento superficial y recarga hídrica, lo cual implica que variaciones en este parámetro están íntimamente vinculadas al riesgo de erosión y de acumulación de agua en superficie.
Esta ejerce una fuerte influencia sobre la partición de la lluvia en infiltración y escurrimiento (Lozano et al., 2020). Una estimación precisa de la conductividad hidráulica es clave para modelar procesos hidrológicos y de erosión, ya que define la velocidad y dirección del agua en el suelo, afectando el drenaje y la salud radicular (Macías et al., 2018). Esta variable depende de las características propias del suelo, pero sus valores varían según el tipo de uso, ya sea natural o antrópico, y los efectos que dicho manejo ejerce sobre sus propiedades físicas (Castiglion et al., 2018).
Cuantificación de esporas y
porcentaje de micorrización en raíces de Glomeromycetes
El análisis estadístico para el número de esporas en los suelos evaluados y el porcentaje de raíces micorrizadas arrojó los siguientes resultados (Tabla 3).
Tabla 3. Análisis de varianza para la cuantificación de esporas y porcentaje de micorrización
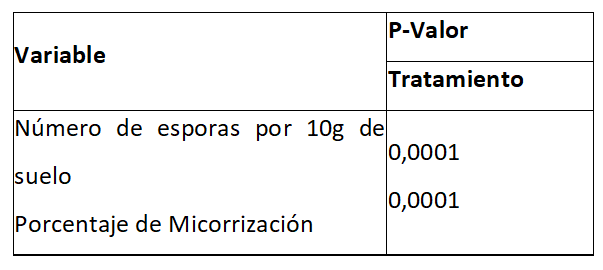
Fuente: elaboración propia
Número de esporas
En la Figura 2 se presentan los resultados obtenidos, donde el mayor número promedio de esporas se registró en el suelo de chagras, con un total de 52, mientras que en el suelo de cultivo de frijol bajo manejo convencional fue de 21 esporas.
Figura 2. Comparación de
esporas micorrízicas arbusculares (HMA) en el suelo asociado a Phaseolus
dumosus y Phaseolus vulgaris
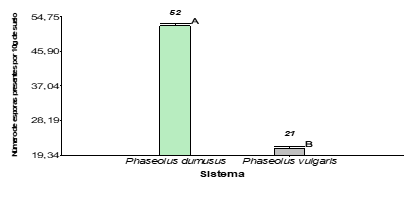
Fuente: elaboración propia
Con respecto a lo señalado por Aguilar et al. (2016), la formación de esporas micorrízicas comienza entre la tercera y cuarta semana tras la colonización de la raíz, con variaciones según la especie vegetal y las condiciones edáficas y ambientales. En este estudio se evidenció una mayor densidad de esporas en sistemas conservados como las chagras, mientras que en monocultivos esta disminuyó debido a la alteración de los ecosistemas, lo que impacta negativamente la abundancia y composición de las micorrizas arbusculares.
Los resultados indican que los sistemas de chagra tienen más esporas que los suelos bajo manejo convencional, lo que se atribuye a las prácticas agrícolas de cada sistema (Lozano et al., 2015). Los valores de porcentaje de micorrización determinaron que existen diferencias significativas al (P<0,005) entre las raíces, se determinó que las de la chagra tradicional donde se maneja (Phaseolus dumosus) con 88,64 % y las raíces del frijol con manejo convencional (Phaseolus vulgaris ) con 53,71 %.
Según lo observado en la Figura 3, el sistema de conservación, (Phaseolus dumusus) presenta el mayor porcentaje de micorrización con 88,64 %. Este elevado nivel de colonización en las raíces indica que una gran proporción de ellas está asociada con hongos micorrízicos. Dicha asociación puede aportar múltiples beneficios a las plantas, entre ellos una mejor absorción de nutrientes, mayor tolerancia al estrés y una mayor resistencia frente a enfermedades (Muñoz et al., 2009).
Figura 3. Porcentaje de
micorrización en dos sistemas de manejo de frijol
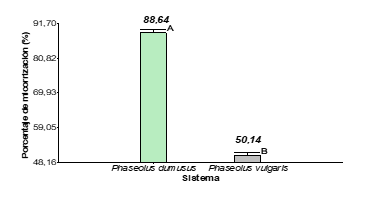
Fuente: elaboración propia
A diferencia con el sistema de chagra, el sistema convencional representado por Phaseolus vulgaris mostró el menor porcentaje de micorrización, con un valor de 50,14 %. Este nivel relativamente bajo de colonización micorrízica sugiere una menor interacción entre las raíces y los hongos micorrízicos arbusculares. Como consecuencia, es probable que las plantas bajo este sistema tengan una capacidad reducida para absorber ciertos nutrientes esenciales, así como una menor tolerancia al estrés ambiental y una resistencia disminuida frente a enfermedades. Este resultado puede estar asociado a prácticas agrícolas intensivas o al manejo del suelo que limita el desarrollo de asociaciones simbióticas beneficiosas, afectando negativamente la salud y productividad del cultivo (Ley Rivas et al., 2015).
Molina et al. (2005) afirman que, porcentaje de micorrización es reflejo de una simbiosis efectiva que mejora la absorción de nutrientes como fósforo y nitrógeno, incrementa la resistencia de las plantas al estrés biótico, abiótico y favorece el crecimiento radicular. A pesar de que la densidad de esporas en el suelo rizosférico fue considerada media, esto no impidió que se alcanzaran altos niveles de colonización, lo que resalta que no siempre existe una correlación directa entre la cantidad de esporas presentes en el suelo y el grado de colonización radicular.
Durante las observaciones microscópicas de raíces teñidas, se identificaron distintas estructuras asociadas a la simbiosis micorrízica arbuscular. En la Figura 4A, 4B y 4D Se observan hifas intracelulares que penetran las células corticales de la raíz, facilitando un intercambio de nutrientes: el hongo provee fósforo y minerales, mientras la planta aporta compuestos carbonados. Estas estructuras aumentan la eficiencia en la absorción de nutrientes esenciales (Smith y Read, 2008). En la Figura 4C se observan vesículas, estructuras globosas u ovoides que actúan como reservas energéticas y permiten la supervivencia del hongo en condiciones adversas, así como la colonización de nuevas raíces (Nardini et al., 2011). En la imagen D se observan hifas intracelulares, filamentos fúngicos que penetran las células corticales de la raíz y establecen una conexión íntima entre el hongo y la planta, facilitando el intercambio bidireccional de nutrientes: el hongo aporta fósforo y minerales, y la planta compuestos carbonados. Estas hifas pueden ramificarse formando arbúsculos, esenciales en este proceso (Callejas et al., 2009).
Figura 4. Raíces micorrizadas
observadas al microscopio a diferentes aumentos: (A y B) con objetivo de 4X,
(C) con objetivo de 10X y (D) con objetivo de 40X, con un ocular de 10X
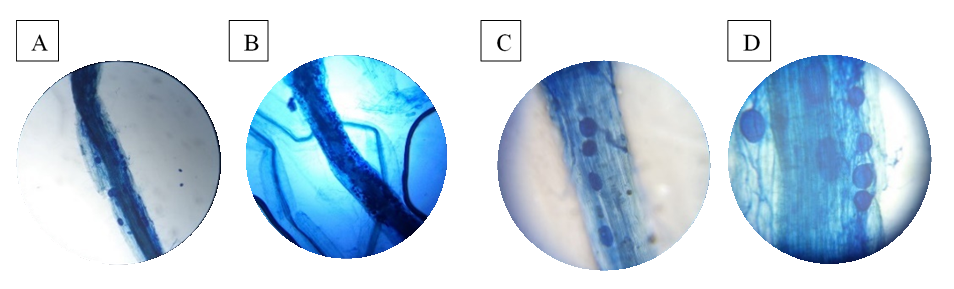
Fuente: elaboración propia.
Según Álvarez et al. (2022) el 85 % de las plantas terrestres forman asociaciones mutualistas con hongos micorrízicos, lo que les permite mejorar la absorción de nutrientes, resistir sequías y ataques de patógenos, dependiendo de su morfología y familia. A cambio, la planta hospeda al hongo, proporcionándole compuestos fotosintéticos y un hábitat protegido.
En suelos ácidos o de baja fertilidad, las micorrizas mejoran la absorción de fósforo (Garzón, 2016), ya que los hongos micorrízicos arbusculares extienden el sistema de absorción más allá de la zona de raíces y permiten que las plantas capten más fósforo incluso cuando la disponibilidad es reducida (Li et al., 2006). Aunque no fijan nitrógeno por sí solas, pueden facilitar su fijación al interactuar con otros microorganismos del suelo (Mosquera et al., 2010), como sucede en leguminosas donde la micorriza mejora la nutrición fósforo del hospedero y con ello incrementa la eficiencia de fijación biológica de nitrógeno (Püschel et al., 2017)
Además, promueven mayor tamaño y producción de semillas, y la liberación de fitohormonas que mejoran la estructura del suelo, aumentando la resistencia de la planta a plagas y sequía (Molina et al., 2005). En efecto, estudios han demostrado que la inoculación con micorrizas incrementa la biomasa vegetal, la eficiencia de uso del fósforo y la tolerancia a condiciones de estrés abiótico (Wu et al., 2024)
Conclusiones
Los resultados mostraron diferencias significativas en las propiedades físicas de los suelos entre los dos sistemas de manejo agrícola evaluados. El suelo de las chagras tradicionales presentó una mayor densidad aparente y real en comparación con el cultivo convencional, lo que indica una estructura más compacta, pero sin diferencias en porosidad y humedad gravimétrica. Ambos suelos favorecen el desarrollo de micorrizas, aunque los suelos convencionales podrían mejorar en aireación y retención de humedad gracias a prácticas que aumentan la materia orgánica.
La cuantificación de esporas mostró una mayor abundancia en los suelos de conservación, con un promedio de 52 esporas frente a las 21 en los suelos agrícolas convencionales, lo que sugiere que los sistemas tradicionales favorecen la proliferación de hongos micorrízicos. El uso intensivo de los suelos en la agricultura convencional limita la diversidad y abundancia de estos hongos beneficiosos. El porcentaje de micorrización en raíces fue notablemente más alto en Phaseolus dumosus cultivado en chagras tradicionales (88,64 %) en comparación con Phaseolus vulgaris en suelos convencionales (50,14 %), lo que resalta la importancia de prácticas agrícolas menos agresivas para mejorar las asociaciones simbióticas y la absorción de nutrientes, tolerancia al estrés y resistencia a enfermedades en las plantas.
Referencias bibliográficas
Aguilar-Ulloa, W., Arce-Acuña, P., Galiano-Murillo, F., y Torres-Cruz, T. J. (2016). Aislamiento de esporas y evaluación de métodos de inoculación en la producción de micorrizas en cultivos trampa. Tecnología en Marcha, 29(3). https://www.scielo.sa.cr/scielo.php?script=sci_arttext&pid=S0379-39822016000700005
Álvarez, J., Solís, A., Villarruel, J., Ortega, M., Garibay, R. (2022). Micorrizas del bosque tropical caducifolio y otras simbiosis fúngicas. Acta Botánica Mexicana, (128). https://doi.org/10.21829/abm128.2021.1906
Barrera, S. (2009). El uso de hongos micorrízicos arbusculares como una alternativa para la agricultura. Biotecnología en el Sector Agropecuario y Agroindustrial, 7(1), 123-131.
Bello Torres, J.V. (2016). El valle de Sibundoy y su transformación agropecuaria 1966-1986. http://hdl.handle.net/20.500.12324/29889
Borie, F. R., Rubio, R., Morales, A., y Castillo, C. (2000). Relación entre densidad de hifas de hongos micorrizógenos arbusculares y producción de glomalina con las características físicas y químicas de suelos bajo cerolabranza. Revista Chilena de Historia Natural, 73(4). http://dx.doi.org/10.4067/S0716-078X2000000400017
Callejas Ruiz, B., Castillo González, A., Colinas León, M., González Chávez, M. C. Pineda Pineda, J., Valdez Aguilar, L. (2009). Sustratos y hongos micorrízicos arbusculares en la producción de nochebuena. Revista Chapingo Horticultura, 15(1).
Carrillo-Saucedo, S.M., Puente-Rivera, J., Montes-Recinas, S., y Cruz-Ortega, R. (2022). Las micorrizas como una herramienta para la restauración ecológica. Acta Botánica Mexicana, (129). https://doi.org/10.21829/abm129.2022.1932
Casanoves, F., Macchiavelli, R., Balzarini, M., y Di Rienzo, J.A. (2022). Modelos no lineales mixtos: aplicaciones en InfoStat. https://repositorio.catie.ac.cr/bitstream/handle/11554/11757/BCO22058365e.pdf?sequence=1yisAllowed=n
Castiglion, G., Behrends, F., Marquez, J. (2018). Conductividad hidráulica saturada determinada por distintos procedimientos en suelos con alta humedad inicial. Ciencia del Suelo, 36(2). https://www.scielo.org.ar/scielo.php?script=sci_arttext&pid=S1850-20672018000200015
Cicore, P., Sánchez, R., Peralta, R., Franco, C., Aparicio, C., Costa, L. (2015). Delimitación de ambientes edáficos en suelos de la pampa deprimida mediante la conductividad eléctrica aparente y la elevación. Ciencia del suelo, 33(2), 229-237.
Coorpoamazonia. (2007). Plan de Manejo Ambiental de los Humedales de la parte plana del Valle de Sibundoy. https://www.corpoamazonia.gov.co/images/Publicaciones/30%202006_PMA_Humedales_Valle_Sibundoy/2006_PMA_humedales_Valle_de_sibundoy.pdf
Correa, O., De la Fuente, E., Carmona, M. Kantolic, A. G., Lavado, R. S. (Eds.). (2011). Soja: Investigación científico-técnica desarrollada en el INBA (Conicet/Fauba), Buenos Aires, Facultad de Agronomía de la UBA. Universidad de Buenos Aires.
Deepika, S., Kothamasi, D. (2014). Soil moisture—A regulator of arbuscular mycorrhizal fungal community assembly and symbiotic phosphorus uptake. Mycorrhiza, 25(1), 67-75. https://doi.org/10.1007/s00572-014-0596-1
Derkowska, E., Sas Paszt, L., & Beata Sumorok, B. D. (2015). Assessment of Mycorrhizal Frequency in the Roots of Fruit Plants Using Different Dyes. https://www.scirp.org/reference/ReferencesPapers?ReferenceID=1398644
Donald, G., Lobo, D., y Mansonia, M. P. (2011). Métodos para determinar la conductividad hidráulica saturada y no saturada de los suelos. Venesuelos, 14(1), Article 1. https://saber.ucv.ve/ojs/index.php/rev_venes/article/view/980
Drew, E. A., Murray, R. S., Smith, S. E., y Jakobsen, I. (2003). Beyond the rhizosphere: Growth and function of arbuscular mycorrhizal external hyphae in sands of varying pore sizes. Plant and Soil, 251(1), 105-114. https://doi.org/10.1023/A:1022932414788
Falcón, E., López, M., Bonilla, M., Rodríguez, O. (2021). Efecto del sustrato y la micorriza arbuscular en el sistema radical y estado nutricional de Swietenia mahagoni L. Jacq. Revista Cubana de Ciencias Forestales, 9(3). https://cfores.upr.edu.cu/index.php/cfores/article/view/705
Fernández Pérez, C.J., Cely Reyes, G.E., y Ramírez, P.A. (2019). Cuantificación de la captura de carbono y análisis de las propiedades del suelo en coberturas naturales y una plantación de pino en el páramo de Rabanal, Colombia. Cuadernos de Geografía: Revista Colombiana de Geografía, 28(1) https://doi.org/10.15446/rcdg.v28n1.66152
Fernández-Rodríguez, JP., Álvarez-Herrera, J.G., y Jaime-Guerrero, M. (2024). Propiedades físicas de un suelo sometido a la aplicación de diferentes cantidades de materia orgánica de escarabajo. Revista U.D.C.A y Divulgación Científica, 27(2), 2561. https://doi.org/10.31910/rudca.v27.n2.2024.2561
Florián, P., Roca, D. (2011). Sustratos para el cultivo sin suelo. Materiales, propiedades y manejo. Sustratos, manejo del clima, automatización y control en sistemas de cultivo sin suelo, Bogotá - Universidad Nacional de Colombia. pp. 37-77.
García, C., Pachepsky, Y., y Martín, M. Á. (2018). Technical note: Saturated hydraulic conductivity and textural heterogeneity of soils. Hydrology and Earth System Sciences, 22(7), 3923–3932. https://doi.org/10.5194/hess-22-3923-2018
Garzón, L.P. (2016). Importancia de las micorrizas arbusculares (ma) para un uso sostenible del suelo en la amazonia colombiana. Revista Luna Azul, (42), 1909-2474. https://doi.org/10.17151/luaz.2016.42.14
Giap, S. G. E., y Ahmad, M. F. (2024). Factors Affecting Soil Bulk Density: A Conceptual Model. Journal of Soil, Environment y Agroecology, 1(1), 27-45. https://doi.org/10.37934/sea/1.1.2745a
Gómez, M., Lindig-Cisneros, R., Cruzado-Vargas, A. L., Gómez-Romero, M., Lindig-Cisneros, R., Cruzado-Vargas, A. L. (2024). Efectos de la aplicación de ácido orgánico y simbiosis ectomicorrízica sobre el crecimiento y parámetros morfológicos de Pinus pseudostrobus. https://www.scielo.org.mx/scielo.php?script=sci_arttext&pid=S2007-42982024000300843&lang=es
González Barrios, J.L., González Cervantes, G., Sánchez Cohen, I., López Santos, A., Valenzuela Núñez, M. (2011). Caracterización de la porosidad edáfica como indicador de la calidad física del suelo. Terra Latinoamericana, 29(4). https://www.scielo.org.mx/scielo.php?script=sci_arttext&pid=S0187-57792011000400369
González Chávez, A., Gutiérrez Castorena, C., Wright, S. (2015). Hongos micorrízicos arbusculares en la agregación del suelo y su estabilidad. Terra Latinoamericana, 22(4), 507-514. https://www.redalyc.org/pdf/573/57311096014.pdf
Gryndler, M., Hršelová, H., Cajthaml, T., Havránková, M., Řezáčová, V., Gryndlerová, H., y Larsen, J. (2009). Influence of soil organic matter decomposition on arbuscular mycorrhizal fungi in terms of asymbiotic hyphal growth and root colonization. Mycorrhiza, 19(4), 255-266. https://doi.org/10.1007/s00572-008-0217-y
Guerrero, E. (2009). Micorrizas: Recurso biológico del suelo. Fondo FEN Colombia. Universidad de Cornell, pp 208.
Guerreo Forero, E. G., y Azcon, C. (1996). Micorrizas: Recurso biológico del suelo. Fondo FEN Colombia. https://books.google.com.co/books?id=nftEAAAAYAAJ
Hossne, G., A. (2008). La densidad aparente y sus implicaciones agrícolas en el proceso expansión/contracción del suelo. Terra Latinoamericana, 26(3). https://www.scielo.org.mx/scielo.php?script=sci_arttext&pid=S0187-57792008000300001
Howeler, R., & Sieverding, E. (2021). 1982-2 (52) Howeler & Sieverding La importancia de las micorrizas en la absorción de fosforo por yuca. 12, 182-195.
Kefan, X., Garzón, L., Xiuling, Y., Yifei, J., Jingchun, Renhao, J., Can, J., y Jianli, L. (2022). Effects of different organic amendments on soil pore structure acquired by three‐dimensional investigation. 73(4). https://doi.org/10.1111/ejss.13264
Li, H., Smith, S. E., Holloway, R. E., Zhu, Y., y Smith, F. A. (2006). Arbuscular mycorrhizal fungi contribute to phosphorus uptake by wheat grown in a phosphorus-fixing soil even in the absence of positive growth responses. New Phytologist, 172(3), 536-543. https://doi.org/10.1111/j.1469-8137.2006.01846.x
Lima, J. S. S., Bezerra-Neto, F., Negreiro, M. Z., Ribeiro, M. C. C., y Barros-Júnior, A. P. (2010). Productive performance of carrot and rocket cultivars in strip-intercropping system and sole crops. https://www.scielo.org.mx/scielo.php?script=sci_arttext&pid=S1405-31952010000500006
Lozano Sánchez, J.D., Armbrecht, I., Montoya Lerma, J. (2015). Hongos formadores de micorrizas arbusculares y su efecto sobre la estructura de los suelos en fincas con manejos agroecológicos e intensivos. Acta Agronómica, 64(4), 2323-0118. http://dx.doi.org/10.15446/acag.v64n4.46045
Lozano-Trejo, S., Olazo Aquino, J., Pérez León, I., Castañeda-Hidalgo, E., Díaz-Zorrilla, O., Santiago-Martínez, M. (2020). Infiltración y escurrimiento de agua en suelos de una cuenca en el sur de México. Tierra Latinoamericana, 38(1). https://doi.org/10.28940/terra.v38i1.443
Macías, J., Vargas, A., Arellano, F. (2018). Conductividad hidráulica en dos sitios del Valle Central de Costa Rica: Análisis comparativo de tres metodologías de ensayo en la zona no saturada. Revista Geológica de América Central, 59(1), 75-100. https://www.scielo.sa.cr/scielo.php?script=sci_arttext&pid=S0256-70242018000200071
Martínez, P., y Roca, D. (2011). Sustratos para el cultivo sin suelo. Materiales, propiedades y manejo. En R. V. J. Flórez (Ed.), Sustratos, manejo del clima, automatización y control en sistemas de cultivo sin suelo (pp. 37–77). Universidad Nacional de Colombia — Editorial Unibiblos. https://redivia.gva.es/handle/20.500.11939/3894
McGrath, D., y Henry, J. (2016). Organic amendments decrease bulk density and improve tree establishment and growth in roadside plantings. Urban Forestry y Urban Greening, 20, 120-127. https://doi.org/10.1016/j.ufug.2016.08.015
Molina, M., Mahecha, L., Medina, M. (2005). Importancia del manejo de hongos micorrizógenos en el establecimiento de árboles en sistemas silvopastoriles. Revista Colombiana de Ciencias Pecuarias, 18(2). https://revistas.udea.edu.co/index.php/rccp/article/view/324004/20781184
Ley Rivas, J. F., Sánchez, J. A., Ricardo, N. E., y Collazo, E. (2015). Efecto de cuatro especies de hongos micorrizógenos arbusculares en la producción de frutos de tomate. Agronomía Costarricense, 39(1). https://doi.org/10.15517/rac.v39i1.19544
Llique Mondragón, R.H. (2015). Influencia de la humedad de compactación en el comportamiento volumétrico de los suelos arcillosos [Tesis de doctorado, Universidad Nacional de Trujillo]. https://repositorio.unitru.edu.pe/entities/publication/d1e95123-2b4f-409e-ad90-c6036a7cdfd6
Mosquera, T., Bayman, P., Otero, T. (2010). Ceratobasidium como hongo micorrízico de orquídeas en Colombia. Acta Agronómica, 59(3). http://www.scielo.org.co/scielo.php?script=sci_arttext&pid=S0120-28122010000300007
Muñoz, E., Macías, C., Franco, A., Sánchez, E., Jiménez, J., González, J. (2009). Identificación y colonización natural de hongos micorrízicos arbusculares en nogal. Terra Latinoamericaca, 27(4). https://www.scielo.org.mx/scielo.php?script=sci_arttext&pid=S0187-57792009000400010
Nardini, B., Di Salvo, P., García-de Salamone, I. (2011). Micorrizas arbusculares: Asociaciones simbióticas e indicadores de calidad ambiental en sistemas de cultivos extensivos. Revista Argentina de Microbiología, 43(4). https://www.redalyc.org/pdf/2130/213021188011.pdf
Nieto, J., y Chegwin, C. (2010). Influencia del sustrato utilizado para el crecimiento de hongos comestibles sobre sus características nutraceúticas. Revista Colombiana de Biotecnología, 12(1), 169-178. https://www.redalyc.org/articulo.oa?id=77617786016
Noda, Y. (2009). Las Micorrizas: Una alternativa de fertilización ecológica en los pastos. Pastos y Forrajes, 32(2), 1-10. https://www.redalyc.org/articulo.oa?id=269119695001
Organización de las Naciones Unidas para la Alimentación y la Agricultura. (s.f.). Planificación y realización de un levantamiento de Suelos. En Colección FAO Capacitación. https://www.fao.org/fishery/static/FAO_Training/FAO_Training/General/x6706s/Index.htm
Osorio, C. A. R., Calle, C. M., & Calle, C. A. Á. (2019). Micorrizas Arbusculares. Libros y Manuales. 52(79). https://doi.org/10.38141/10791/0005_3
Osorio, N.W. (2012). Uso de hongos formadores de micorriza como alternativa biotecnológica para promover la nutrición y el crecimiento de plantulas. 1(2). https://www.bioedafologia.com/sites/default/files/documentos/pdf/Hongos-formadores-de-micorrizas.pdf
Pauwels, R., Graefe, J., y Bitterlich, M. (2023). An arbuscular mycorrhizal fungus alters soil water retention and hydraulic conductivity in a soil texture specific way. Mycorrhiza, 33(3), 165-179. https://doi.org/10.1007/s00572-023-01106-8
Pérez, A., y Vertel, M. (2010). Evaluación de la colonización de micorrizas arbusculares en pasto Bothriochloa pertusa (L) A. Camus. Revista MVZ Córdoba, 15(3). http://www.scielo.org.co/scielo.php?script=sci_arttext&pid=S0122-02682010000300004
Pire, R., y Pereira, A. (2003). Propiedades físicas de componentes de sustratos de uso común en la horticultura del estado lara, Venezuela. Propuesta metodológica. Biagro, 15(1). https://ve.scielo.org/scielo.php?script=sci_arttext&pid=S1316-33612003000100007
Pino, E., Montalván, I., Vera, A., Ramos, L. (2019). La conductancia estomática y su relación con la temperatura foliar y humedad del suelo en el cultivo del olivo (Olea europaea L.), en periodo de maduración de frutos, en zonas áridas.La Yarada, Tacna, Perú. Idesia (Arica), 37(4), 0718-3429. http://dx.doi.org/10.4067/S0718-34292019000400055
Püschel, D., Janoušková, M., Voříšková, A., Gryndlerová, H., Vosátka, M., y Jansa, J. (2017). Arbuscular Mycorrhiza Stimulates Biological Nitrogen Fixation in Two Medicago spp. Through Improved Phosphorus Acquisition. Frontiers, 8. https://doi.org/10.3389/fpls.2017.00390
Salamanca Jiménez, A., y Sadeghian Khalajabadi, S. (2005). La densidad aparente y su relación con otras propiedades en Suelos de la zona cafetera colombiana. Cenicafé, 56(4), 381-397.
Shao, Y., Wang, Z., Liu, W., Zhang, X., Wang, J., y Guo, P. (2023). Effects of Variations in Soil Moisture and Phosphorus Concentrations on the Diversity of the Arbuscular Mycorrhizal Fungi Community in an Agricultural Ecosystem. Agriculture, 13(6), 1272. https://doi.org/10.3390/agriculture13061272
Smith, S., y Read, D. (2008). Assessment of mycorrhizal frequency in the roots of fruit plants using different dyes. En Mycorrhizal Symbiosis (3.a ed.). Academic Press. https://doi.org/10.1016/B978-0-12-370526-6.X5001-6
Steponavičienė, V., Bogužas, V., Sinkevičienė, A., Skinulienė, L., Vaisvalavičius, R., y Sinkevičius, A. (2022). Soil Water Capacity, Pore Size Distribution, and CO2 Emission in Different Soil Tillage Systems and Straw Retention. Plants, 11(5), 614. https://doi.org/10.3390/plants11050614
Wang, X., Liu, E., Wang, L., y Lv, P. (2025). Changes in Soil Physical Properties and Maize Productivity in Response to Nitrogen Substitution by Maize Stover for Mineral Fertilizers. Agronomy, 15(3), 587. https://doi.org/10.3390/agronomy15030587
Wu, Y., Chen, C., y Wang, G. (2024). Inoculation with arbuscular mycorrhizal fungi improves plant biomass and nitrogen and phosphorus nutrients: A meta-analysis. BMC Plant Biology, 24(1), 960. https://doi.org/10.1186/s12870-024-05638-9
1 Ingeniera Ambiental, Institución Universitaria del Putumayo - UNIPUTUMAYO. Colón, Colombia. Correo electrónico: jeimyortega2020@itp.edu.co - ORCID: https://orcid.org/0009-0006-5704-1139 - Google Scholar: https://scholar.google.com/citations?hl=es&user=CfrA5IoAAAAJ
2 Ingeniera Ambiental, Institución Universitaria del Putumayo - UNIPUTUMAYO. Colón Colombia. Correo electrónico: yulinaarcos2020@itp.edu.co - ORCID: https://orcid.org/0009-0009-7768-3958 - Google Scholar: https://scholar.google.com/citations?hl=es&user=PhFHU4UAAAAJ
3 Magister en ciencias Agrarias, Especialista en Gerencia Ambiental, Ingeniera Agrónoma. Docente, Institución Universitaria del Putumayo - UNIPUTUMAYO. Colón, Colombia. Correo electrónico: aguerra@itp.edu.co ORCID: https://orcid.org/0000-0002-9731-8933 Google Scholar: https://scholar.google.com/citations?hl=es&user=niS_PY4AAAAJ
4 Ingeniero Ambiental, Institución Universitaria del Putumayo - UNIPUTUMAYO, Colón, Colombia. Correo electrónico: brayanarleyerazo2020@itp.edu.co - ORCID: https://orcid.org/0009-0009-4599-5041- Google Scholar: https://scholar.google.com/citations?hl=es&user=i4n0X3UAAAAJ
Para citar este artículo: Ortega Urbano, J.J., Arcos Rodríguez, Y., Guerra Acosta, A.S., y Erazo Guerrero, B.A. (2026). Evaluación de las propiedades físicas del suelo y presencia de micorrizas arbusculares en dos sistemas de cultivos de frijol (Phaseolus vulgaris y Phaseolus dumosus) en Sibundoy, Putumayo. Revista Luna Azul, (62), 170-188. DOI: https://doi.org/10.17151/luaz.2026.62.10
Esta obra está bajo una Licencia de Creative Commons Reconocimiento CC BY
Código
QR del artículo
